(单选题)
下列电池中,电池的电动势与Cl-的活度无关的是()。
A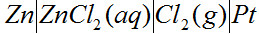
B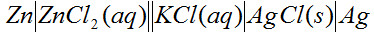
C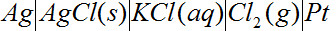
D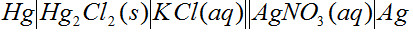
正确答案
答案解析
略
相似试题
(单选题)
下列电池中,哪个电池的电动势与 Cl-离子的活度无关?()
(单选题)
今有电池:(-)Pt│Cr2O72-,H+,Cr3+‖Cl-│Cl2(g),Pt(+),要增加电池电动势的办法是()
(简答题)
由标准钴电极(Co2+/Co)与标准氯电极组成原电池,测得其电动势为1.64V,此时钴电极为负极。已知φΘ(Cl2/Cl-)=1.36V,问: (l)标准钴电极的电极电势为多少?(不查表) (2)此电池反应的方向如何? (3)当氯气的压力增大或减小时,原电池的电动势将发生怎样的变化? (4)当Co2+的浓度降低到0.010mol˙L-1时,原电池的电动势将如何变化?数值是多少?
(简答题)
将反应Ag(s)+1/2Cl2(g)=AgCl(s)设计成原电池,已知在25℃时 , ,标准电极电势EΘ(Ag+│Ag)=0.7994V,EΘ(Cl-│Cl2(g)│Pt)=1.3579V。 (1)写出电极反应和电池图示; (2)求25℃时电池可逆放电2F电荷量时的热Qr; (3)求25℃时AgCl的活度积。
(简答题)
已知Eθ(Pb2+/Pb)=-0.126V,Eθ(Fe3+/Fe2+)=0.771V,Kθsp(PbCl2)=1.6×10-5。在金属铅和硝酸铅溶液组成的半电池系统中,加入NaCl(aq)。当c(Cl-)=1.0mol·L-1时,该半电池的电极电势是多少?将该半电池与Fe3+/Fe2+标准半电池组成原电池。写出电池反应的离子方程式,并计算此原电池的标准电动势Eθ。
(单选题)
Li - Cl2电池结构如下: Li│LiCl((饱和液)有机溶剂)│Cl2(pθ)│Pt已知ΔfGmθ[LiCl(s)]=-384kJ/mol,则该电池的电动势值E为:()
(简答题)
电池Pt|H2(101.325kPa)|HCl(0.10mol•kg-1)|Hg2Cl2(s)|Hg电动势E与温度T的关系为:E/V=0.0694+1.881×10-3T/K-2.9×10-6(T/K)2。
(简答题)
电池Pt|H2(101.325kPa)|HCl(0.10mol•kg-1)|Hg2Cl2(s)|Hg电动势E与温度T的关系为:E/V=0.0694+1.881×10-3T/K-2.9×10-6(T/K)2。
(简答题)
电池Pt|H2(101.325kPa)|HCl(0.10mol•kg-1)|Hg2Cl2(s)|Hg电动势E与温度T的关系为:E/V=0.0694+1.881×10-3T/K-2.9×10-6(T/K)2。


