(简答题)
AgI饱和的0.020mol.L-1NaI溶液达到平衡后组成下列电池:测得电动势为0.048V,计算AgI的溶度积常数Ksp?(φθAg+/Ag=+0.779V) 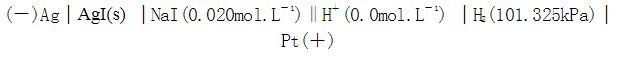
正确答案

答案解析
略
相似试题
(单选题)
在0.20mol.L-1Na[Ag(CN)2]溶液中,加入等体积水稀释,下列那种粒子的浓度变为0.10mol.L-1()
(简答题)
计算下列溶液的pH值:0.20mol·L-1Na2CO3溶液与0.10mol·L-1HCl溶液等体积混合。
(简答题)
40mlc(Na2HPO4)=0.10mol·L-1Na2HPO4水溶液与20mlc(H3PO4)=0.10mol·L-1H3PO4水溶液混合,混合液的pH是多少?
(简答题)
将一定量的MnO2加入过量盐酸中,生成的氯气通入KI溶液中游离出的碘恰被20ml0.1mol·L-1Na2S2O3滴定,求MnO2的质量(MnO2的分子量为87)
(简答题)
用碘量法测定葡萄糖的含量。准确10.00g称取试样溶解后,定容于250mL容量瓶中,移取50.00mL试液于碘量瓶中,加入0.05000mol·L-1I2溶液30.00mL(过量的),在搅拌下加入40mL0.1mol·L-1NaOH溶液,摇匀后,放置暗处20min。然后加入0.5 mol·L-1HCl8mL,析出的I2用0.1000 mol·L-1Na2S2O3溶液滴定至终点,消耗9.96mL。计算试样中葡萄糖的质量分数。
(简答题)
称取丙酮试样1.000g,定容于250mL容量瓶中,移取25.00mL于盛有NaOH溶液的碘量瓶中,准确加入50.00mL 0.05000mol.L-1I2标准溶液,放置一定时间后,加H2SO4调节溶液呈弱酸性,立即用0.1000 mol.L-1Na2SO4溶液滴定过量的I2,消耗10.00mL。计算试样中丙酮的质量分数。
(简答题)
试剂厂生产的试剂FeCl3·6H2O,根据国家标准GB1621--1979规定其一级品含量不少于96.00%,二级品含量不少于92.00%。为了检查质量,称取0.5000g试样,溶于水,加浓HCl溶液3mL和KI 2g,最后用0.1000mol·L-1Na2S2O3标准溶液18.17mL滴定至终点。计算说明该试样符合哪级标准?
(简答题)
称取含有As2O3与As2O5的试样1.500g,处理为含AsO33-和AsO43-的溶液。将溶液调节为弱碱性,以0.05000mol.L-1碘溶液滴定至终点,消耗30.00 mL。将此溶液用盐酸调节至酸性并加入过量KI溶液,释放出的I2再用0.3000mol.L-1Na2S2O3溶液滴定至终点,消耗30.00mL。计算试样中As2O3与As2O5的质量分数。
(单选题)
AgI在0.010mol•L-1KI溶液中的溶解度为()(已知AgI的Ksp=9.3×10-17)