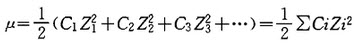 式中,μ:溶液的离子强度;Ci:某种离子的摩尔浓度;Zi:某种离子的化合价;CiZi2:某种离子的摩尔浓度及其化合价平方的乘积;∑:算式中各项数值相加。
式中,μ:溶液的离子强度;Ci:某种离子的摩尔浓度;Zi:某种离子的化合价;CiZi2:某种离子的摩尔浓度及其化合价平方的乘积;∑:算式中各项数值相加。 (简答题)
如何计算溶液的离子强度?
正确答案
溶液的离子强度是指溶液中各离子的摩尔浓度与离子价数平方值的乘积总和的1/2。计算公式是: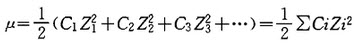 式中,μ:溶液的离子强度;Ci:某种离子的摩尔浓度;Zi:某种离子的化合价;CiZi2:某种离子的摩尔浓度及其化合价平方的乘积;∑:算式中各项数值相加。
式中,μ:溶液的离子强度;Ci:某种离子的摩尔浓度;Zi:某种离子的化合价;CiZi2:某种离子的摩尔浓度及其化合价平方的乘积;∑:算式中各项数值相加。
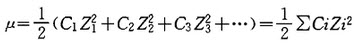 式中,μ:溶液的离子强度;Ci:某种离子的摩尔浓度;Zi:某种离子的化合价;CiZi2:某种离子的摩尔浓度及其化合价平方的乘积;∑:算式中各项数值相加。
式中,μ:溶液的离子强度;Ci:某种离子的摩尔浓度;Zi:某种离子的化合价;CiZi2:某种离子的摩尔浓度及其化合价平方的乘积;∑:算式中各项数值相加。 答案解析
略
相似试题
(判断题)
溶液的离子强度越高,质点的泳动速度越慢。
(判断题)
溶液pH就是氢离子浓度。
(填空题)
PH=6的溶液中氢离子浓度是()mmol/L,溶液显()性。
(填空题)
溶液的氢离子浓度缩小100倍,PH值的变化是: ()。
(单选题)
在0.001mol/L的氯化钡溶液中钡离子与氯离子的浓度相比是:()
(填空题)
氢离子浓度等于10-3mmol/L时,溶液的PH值是(),氢氧根离子浓度等于10-3mmol/L时,溶液的PH值是()。
(单选题)
在0.1mmol/L的氨水中加入固体氯化铵后溶液的氢离子浓度()
(单选题)
设弱酸HA的电离度为α,0.1mol/L溶液中的氢离子的浓度是:()
(单选题)
10毫升1mmol/L氯化钠与20毫升0.5mmol/L氯化钙溶液混合后,氯离子物质的量浓度是()


