
(简答题)
已知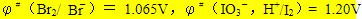 (1)写出标准状态下自发进行的电池反应式; (2)若[Br-] = 0.0001 mol·L-1,而其它条件不变,反应将如何进行? (3)若调节溶液pH=4,其它条件不变,反应将如何进行?
(1)写出标准状态下自发进行的电池反应式; (2)若[Br-] = 0.0001 mol·L-1,而其它条件不变,反应将如何进行? (3)若调节溶液pH=4,其它条件不变,反应将如何进行?
正确答案

答案解析
略
相似试题
(单选题)
某反应在298K标准状态下不能自发进行,但当温度升高到一定值时,反应能自发进行,则符合的条件是()。
(简答题)
写出以下电池的电极反应及电池反应式,并计算25℃时电动势E及ΔrGm,Kθ;并判断电池反应能否自发进行? Pb(s)|Pb(NO3)2[a(Pb2+)=1]||AgNO3[a(Ag+)=1]|Ag(s)(已知:φθ(Pb2+|Pb)=-0.1265V,φθ(Ag+|Ag)=0.7994V)
(单选题)
某一反应,当反应物和产物的活度都等于1时,要使该反应能在电池内自发进行,则:()
(简答题)
根据下列反应组成电池,写出电池组成式,计算298K时的电动势,并判断反应自发进行的方向。
(单选题)
已知电极电位:φ(Cl2|Cl-)=1.36V,φ(Br2|Br-)=1.07V,φ(I2|I-)=0.54V,φ(Fe3+|Fe2+)=0.77V,标准状态下,Fe与卤素组成电池,下面判断正确的是:()。
(判断题)
对于ΔrSθm〉0的反应,标准状态下,高温时正向反应可能自发进行。
(简答题)
计算下列反应在标准状态下,298.15K时的,并判断该条件下反应自发进行的方向。
(填空题)
有A、B、C、D四个反应,在298K时反应的热力学函数分别为 则在标准状态下,任何温度都能自发进行的反应是(),任何温度都不能自发进行的反应是()。
(简答题)
将反应Ag(s)+1/2Cl2(g)=AgCl(s)设计成原电池,已知在25℃时 , ,标准电极电势EΘ(Ag+│Ag)=0.7994V,EΘ(Cl-│Cl2(g)│Pt)=1.3579V。 (1)写出电极反应和电池图示; (2)求25℃时电池可逆放电2F电荷量时的热Qr; (3)求25℃时AgCl的活度积。


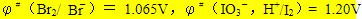 (1)写出标准状态下自发进行的电池反应式; (2)若[Br-] = 0.0001 mol·L-1,而其它条件不变,反应将如何进行? (3)若调节溶液pH=4,其它条件不变,反应将如何进行?
(1)写出标准状态下自发进行的电池反应式; (2)若[Br-] = 0.0001 mol·L-1,而其它条件不变,反应将如何进行? (3)若调节溶液pH=4,其它条件不变,反应将如何进行? 